研究人員揭示病毒RdRP核苷酸添加循環新機制
2023-01-09分子生物學
RNA病毒包括多種致病病原,對人類健康構成威脅。RNA病毒的基因組復制和轉錄過程需要自身編碼的依賴RNA的RNA聚合酶(RNA-dependent RNA polymerase,RdRP)來主導完成。該過程經歷引發(initiation)、延伸(elongation)和終止(termination)階段,由數以千計的核苷酸添加循環(nucleotide addition cycle,NAC)組成。該循環的機制不僅是了解RNA病毒本質特征的重要內容,而且是發展針對RdRP的抗病毒策略的重要依據。現有關于病毒RdRP的研究表明,每個NAC經歷四個步驟:反應底物NTP進入RdRP活性中心;RdRP活性中心關閉(active site closure);核苷酸轉移(nucleotidyl transfer)反應發生(產物RNA的3’-末端添加一個核苷酸);RdRP向下一位模板核苷酸轉位(translocation)從而開啟下一輪循環。過去十余年間,結構生物學與酶學研究已基本完整勾勒出該NAC的機制,但始終未能準確獲得催化反應(步驟3)即將發生時的RdRP結構信息,因此對于哪些氨基酸殘基在催化反應中發揮關鍵作用存在爭議。
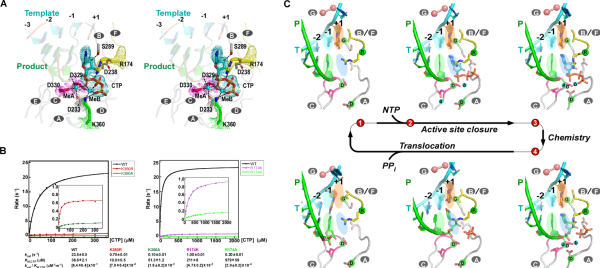
中國科學院武漢病毒研究所研究員龔鵬團隊長期從事病毒RdRP催化機制研究。近期,該團隊通過在腸道病毒71型(enterovirus 71,EV71)RdRP-RNA復合物晶體浸泡實驗中的多方嘗試,解析了高度接近催化反應發生狀態的RdRP晶體結構(圖A,PDB編號:7W9S,分辨率2.5埃),發現位于RdRP基序D附近的一個賴氨酸殘基K360與結構中底物CTP的g-磷酸存在近距離相互作用(3.3埃)。在與EV71同為腸道病毒的脊髓灰質炎病毒的前期研究中,等同的K359殘基被認為直接參與催化反應和其中的質子轉移過程,而上述晶體結構中觀測到的近距離相互作用進一步提示了這種可能性。據此,該團隊選取了EV71 RdRP的K360殘基和另一個與CTP的磷酸基團存在相互作用的基序F精氨酸殘基R174為突變位點設計了系列突變體,利用酶學方法對野生型RdRP和突變體的單步延伸速率常數和CTP米氏常數(圖B)、RdRP延伸狀態(elongation)和延伸前狀態(pre-elongation)下催化的pH依賴性等多種參數和性質進行了表征。結果表明,K360位點的突變降低了催化效率,且在延伸和延伸前狀態下都能影響RdRP的pH依賴特性,而R174位點的突變所造成的影響與K360類似且能額外降低底物CTP的親和力。這些數據表明K360和R174均直接參與催化反應,但這兩個殘基是否直接參與質子轉移有待進一步取證。上述成果是該團隊繼解析RdRP活性中心部分關閉結構(對應NAC步驟2)和揭示不對稱轉位現象(對應NAC步驟4)(PNAS 2016;Nature Communications 2020)等NAC系列工作后的又一成果(對應NAC步驟3),闡明了該循環的全過程機制(圖C、動圖)。
相關研究成果在線發表在《核酸研究》(Nucleic Acids Research)上。研究工作得到國家重點研發計劃、國家自然科學基金、湖北省江夏實驗室生物安全科技重大項目等的支持。
很贊哦! ()