皮下注射“赫賽汀”中國上市,為早期和轉移性 HER2陽性乳腺癌提供機會
能口服不注射,能肌注不靜脈。熱門藥物劑型改良一直是藥物研發的重點方向,抗腫瘤藥物也不例外。10 月 9 日,據 NMPA 官網顯示,羅氏曲妥珠單抗注射液(皮下注射)(商品名:赫賽汀)在國內獲批上市,聯合化療用于治療早期和轉移性 HER2 陽性乳腺癌患者。
皮下注射赫賽汀 給藥僅需5分鐘
2020年6月29日,FDA批準皮下注射劑Phesgo:registered:上市。
Phesgo是羅氏開發的一種皮下注射劑,將帕妥珠單抗(Pertuzumab)、曲妥珠單抗(Trastuzumab)和透明質酸酶(Hyaluronidase)以固定劑量組合的方式聯合起來,在幾分鐘之內就能完成給藥,大大縮短了患者接受治療的時間,與標準的靜脈輸注帕妥珠+曲妥珠+化療方案相比,不僅從5小時縮短成5分鐘,而且操作簡單,疫情期間患者不用去醫院,由專業人士在家或治療中心就能完成,可謂是腫瘤醫學界的一項重大創新!
在 3 期隨機 FeDeriCa 試驗 (NCT03493854) 中,入組的500例患者均為局部晚期或炎性II-IIIC期的HER2陽性可手術的乳腺癌患者,將這些患者按1:1進行隨機分組,給予靜脈輸注帕妥珠單抗(840mg負荷劑量,420mg維持劑量)+曲妥珠單抗(8 mg/kg負荷劑量,6 mg/kg維持劑量)或皮下注射劑Phesgo(1200 mg帕妥珠單抗加600 mg曲妥珠單抗負荷劑量15 mL,然后給予600 mg帕妥珠單抗加600 mg曲妥珠單抗維持劑量10 mL),均每3周給藥一次與新輔助化療一起使用。
結果顯示:皮下注射治療組患者和靜脈輸注治療組患者的病理學完全緩解率幾乎相同,分別為59.7%和59.5%。GMR的90%CI下限為1.14,大于預先規定的非劣效性界限,即血液中藥物濃度相當,同時表現出類似的有效性。此外,Phesgo聯合化療與靜脈注射曲妥珠、帕妥珠單抗和化療的安全性相當,未發現新的安全信號,心臟毒性無顯著差異。
總而言之,Phesgo與靜脈注射曲妥珠、帕妥珠單抗療效相當,安全性相似。但是與靜脈輸注帕妥珠+曲妥珠單抗相比,單次皮下注射Phesgo的給藥速度要快90%以上,大大縮短了給藥時間。
雙抗也能皮下注射 靠譜么?
amivantamab是FDA批準的首個EGFR/c-Met雙抗藥物,2020年7月,強生/楊森已經向CDE申請amivantamab靜脈注射劑型,并在同年9月獲得CDE授予的突破性療法資格。這款EGFR/c-Met雙抗藥物,不但能治療治療EGFR難治突變20ins,在奧希替尼耐藥后產生MET突變的患者中產生很好的療效。6月21日,CDE官網顯示,amivantamab皮下注射劑型在中國申報臨床試驗。相較于靜脈注射,皮下注射給藥更方便,能提高患者的依從性。
于2020年10月披露了一項amivantamab皮下注射劑型治療晚期實體惡性腫瘤的I期臨床研究(NCT04606381,PALOMA研究)。今年AACR大會上公布的I期的PALOMA研究結果顯示,amivantamab皮下注射劑型的使用,具有很好的療效和安全性。

皮下注射的PDL1 夢想照進現實
2021年11月25日,國家藥品監督管理局(NMPA)批準了皮下注射PD-L1抗體恩沃利單抗(KN035)用于標準治療失敗的MSI-H/dMMR晚期結直腸癌、胃癌及其它實體瘤。目前,在中國獲批上市的PD1/L1已經高達10余款,而恩沃利單抗是我國乃至世界首個可皮下注射的PD-L1。
恩沃利單抗是全球首個用于腫瘤免疫治療的單域抗體,是全球第一款皮下注射PD-L1抑制劑。可在30秒內完成給藥,能大幅節約了醫患時間與醫療資源,提高患者依從性。與目前已經上市和在研的PD-(L)1抗體相比,它具有明顯的差異化優勢:安全性良好、可皮下注射、常溫下穩定,可輕松完成給藥過程,大大縮短給藥時間,更好地改善患者生活品質,為實現將腫瘤作為慢性病長期管理的目標邁出了關鍵的一步。
口服化療藥Liporaxel
9月14日,CDE官網顯示,海和藥物和大化制藥合作開發的紫杉醇口服液的上市申請已獲受理,適應癥為二線治療晚期胃癌。

Liporaxel是由DAEHWA Pharmaceuticals韓國大化公司與韓國科學技術研究所(KIST)共同開發的一種紫杉醇口服制劑,其中紫杉醇溶解于"DH-LASED"(DaeHwa–基于脂質的自乳化藥物遞送技術,是DAEHWAPharmaceutical Co.的一項專利技術)。
利用該技術,通過脂類遞送活性成分紫杉醇,解決了造成紫杉醇口服生物利用度低的主要難點。DHP107已于2016年9月9日成功獲得韓國食品與藥品監督局(MFDS)的上市批準,適應癥為晚期和轉移性或局部復發性胃癌,是全球第一個開發成功并獲批上市的口服紫杉醇產品。
海和生物于2017年9月獲得該產品的中國大陸、臺灣、香港及泰國權益,于2018年3月和7月先后遞交胃癌注冊臨床試驗申請和乳腺癌國際多中心III期臨床試驗申請,分別于7月和10月獲得相關批件。
不止口服化療藥 還有口服SERD
Elacestrant(艾拉司群)是Radius公司研發的一款口服選擇性雌激素受體降解劑(SERD),曾在2018年獲得了FDA授予的快速通道資格。2021年10月20日,Menarini /Radius Health宣布口服雌激素受體降解劑elacestrant針對ER+/HER2-晚期或轉移性乳腺癌乳腺患者的的III期EMERALD研究獲得了積極陽性結果!
Elacestrant是首個可以口服的SERD藥物,是一種小分子,它們通過與癌細胞表面的雌激素受體(ER)相結合,降低雌激素受體的穩定性,誘導它們被細胞正常的蛋白降解機制降解,從而降低雌激素受體水平,抑制癌細胞的生長。與抑制雌激素活性的調節劑不同,SERD理論上通過介導雌激素受體的降解,能夠更為全面地抑制雌激素受體的功能,并且可能解決雌激素受體突變產生的耐藥性。
Elacestrant目前正在評估其作為ER+/HER2-晚期乳腺癌患者每日一次口服治療的潛在臨床應用價值。基于之前EMERALD已完成的研究數據表明,Elacestrant以單藥或與其他療法聯合使用在乳腺癌治療領域存在較大發展潛力。
總之,腫瘤治療中,提高藥物療效的同時,提高患者依從性、用藥的便捷性與安全性也是重要的一環,給藥方式的變革也會造福更多腫瘤患者。

- 上一篇

JAMA Surg:微創乳腺手術治療早期乳腺癌患者的長期預后研究
2020年全球腫瘤統計報告顯示,每年全球估計有1930萬例新發腫瘤病例,其中923萬例為女性,女性新發乳腺癌患者226萬例。乳腺癌已經超過肺癌成為發病率最高的腫瘤,是全球腫瘤相關死亡的第五大原因。一項關于全球和區域乳腺癌患者生存率的meta分析顯示,全球乳腺癌患者1年、3年、5年和10年的總生存率分別為92%、75%、73%和61%。乳腺癌需要以手術為主,結
- 下一篇
CDK4/6抑制劑在乳腺癌治療中耐藥機制和改進策略
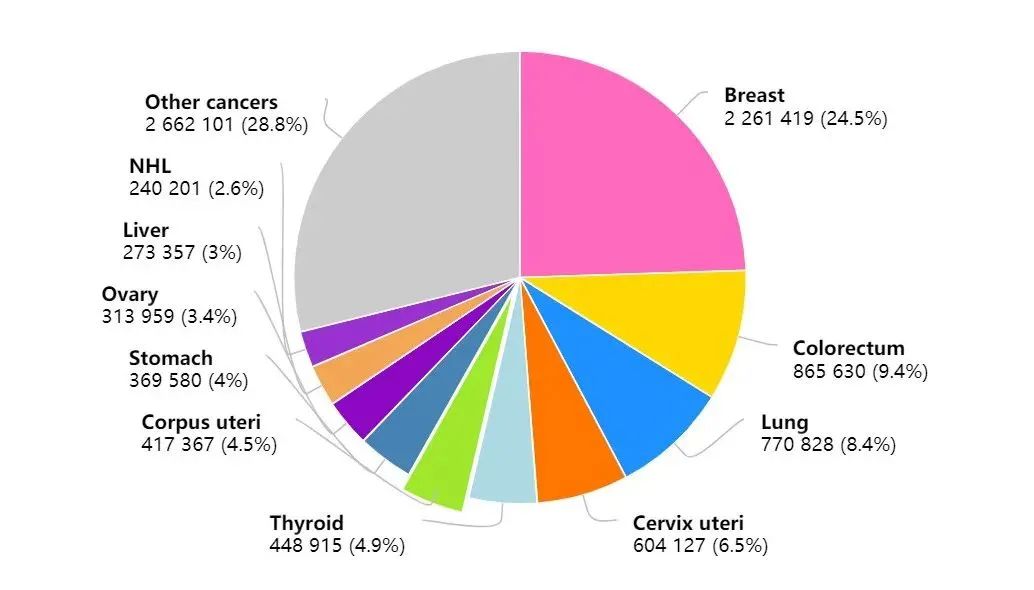
乳腺癌是女性最常見的惡性腫瘤,約占全球所有惡性腫瘤的24.5%。乳腺癌根據雌激素受體(ER)、孕激素受體(PR)和HER2狀態分為三個亞型:激素受體(HR)陽性、HER2陽性和三陰性亞型。其中,HR陽性乳腺癌約占60%–70%。目前,內分泌治療被認為是HR陽性乳腺癌的主要治療方法。盡管晚期疾病的治療有顯著改善,但很大一部分患者最終對內分泌治療產生
