重磅級文章解讀:科學家們在肝癌研究領域取得的新成果!
有研究指出,肝癌在46個國家中是癌癥死亡的三大原因之一,且新發病例和相關死亡率預計未來將會急劇上升;到2040年,預計將有140萬人被診斷為肝癌,肝癌新病例數較2020年將增加55%;到2040年,將有130萬人死于肝癌,肝癌死亡率較2020年也會增加56.4%。
近年來,科學家們在人類肝癌研究領域進行了大量研究,也取得了大量重要的研究成果,本文中,小編就對相關研究進行整理,分享給大家!
【1】Science子刊:衰老的肝星狀細胞觸發肥胖相關肝癌機制
doi:10.1126/sciimmunol.abl7209
在點一份額外的炸薯條之前,需要再考慮一下了。它可能會導致患肝癌的風險增加。作為一種也可能導致肝癌的脂肪性肝病,非酒精性脂肪性肝炎(nonalcoholic steatohepatitis, NASH)的病例在增加,然而有效的治療方法仍然難以找到。
在一項新的研究中,來自日本大阪公立大學和東京理科大學等研究機構的研究人員向抑制和治療NASH相關的肝癌邁出了潛在的一步,他們利用肥胖小鼠的研究解釋了腫瘤微環境中癌細胞附近的細胞膜孔所分泌的蛋白對肝癌產生的重要性,相關研究結果發表在Science Immunology期刊上,論文標題為“Gasdermin D–mediated release of IL-33 from senescent hepatic stellate cells promotes obesity-associated hepatocellular carcinoma”。
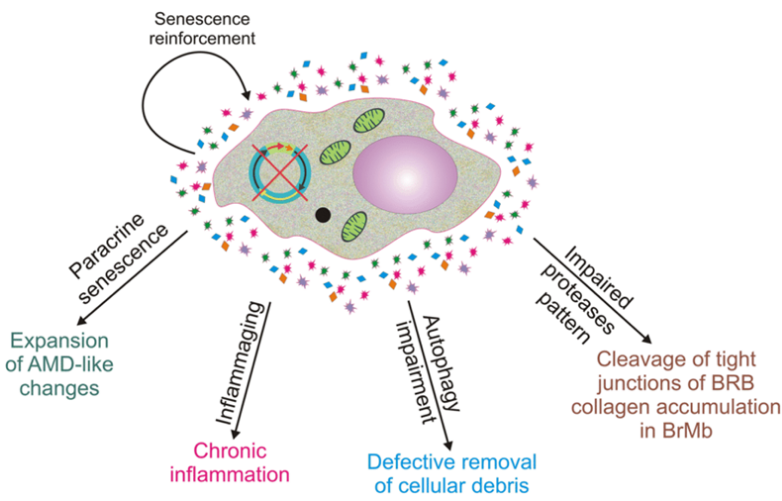
圖片來源:Cellular and Molecular Life Sciences, 2020, doi:10.1007/s00018-019-03420-x。
雖然癌細胞本身顯然是有害的,但鄰近的細胞,包括所謂的“腫瘤微環境”中與癌癥相關的成纖維細胞,也會在癌癥產生中起到一定作用。論文通訊作者Naoko Ohtani教授解釋說,“在肥胖相關的肝臟腫瘤微環境中,稱為‘肝星狀細胞(hepatic stellate cell)’的成纖維細胞變得衰老。”這導致它們表現出衰老相關的分泌表型(SASP),在這種表型中,它們釋放出一系列通過抑制抗腫瘤免疫力來促進癌癥的蛋白。SASP因子等蛋白被釋放出來并加速腫瘤產生的機制仍不清楚。
Ohtani教授及其團隊試圖通過給易患癌癥的小鼠喂食高脂肪飲食并研究肥胖引起的肝癌來揭開這一機制。他們首先進行了全面的基因表達分析,以確定哪些SASP因子是由肝星狀細胞產生的,然后研究它們是如何被釋放出來的;SASP因子IL-1β和IL-33被發現是肝癌生長的兩個關鍵促進因子。它們的釋放主要發生在兩個階段。Ohtani教授闡述說,“首先,高脂肪飲食削弱了腸道屏障功能,導致脂磷壁酸(lipoteichoic acid)在肝臟中遷移和積累。第二,積累的脂磷壁酸刺激了galdermin D蛋白的裂解。這反過來又形成了細胞膜孔,肝星狀細胞通過這些細胞膜孔將IL-1β和IL-33輸出或釋放。”
【2】Hepatology:腫瘤壞死因子-α誘導炎性微環境促進肝癌的發生
doi:10.1002/hep.32738
肝細胞癌仍然是全球癌癥相關死亡的重要原因。肝細胞癌相對隱匿性較強,一般診斷為晚期,預后較差。此外,肝細胞癌的異質性降低了靶向治療的有效性。這些事實促使我們把重點放在預防肝癌上。然而,目前對肝癌發生的機制尚不完全清楚,這極大地限制了肝癌的預防。
越來越多的證據表明,間充質干細胞(MSCs)是肝臟受損局部組織和腫瘤微環境的家園。慢性炎癥被認為是原發性肝癌的主要特征。然而,內源性MSCs在炎癥環境中的特征及其在肝癌發生中的作用尚不清楚。
近日,來自第二軍醫大學附屬第三醫院的研究者們在Hepatology雜志上發表了題為“AIF1 + CSF1R + MSCs, induced by TNF-α, act to generate an inflammatory microenvironment and promote hepatocarcinogenesis”的文章,該研究結果表明,動員到損傷部位的MSCs可以被巨噬細胞培養。反過來,受過刺激的MSCs參與了慢性炎癥微環境的產生和促進肝癌的發生。
在本研究中,研究者采用單細胞RNA測序的方法,鑒定了肝癌發生前存在于微環境中的一個非炎癥相關的MSCs亞群,即AIF1+CSF1R+MSCs。進一步,研究者發現這一MSCs亞群很可能是由腫瘤壞死因子-α刺激通過TNFR1SIRT1途徑誘導的。在大鼠原發性肝癌模型中,研究者發現高表達SIRT1的MSCs(Ad-Sirt1-MSCs)促進巨噬細胞募集,并通過分泌CCL5協同促進肝癌的發生。有趣的是,Ad-Sirt1-MSCs中巨噬細胞的耗盡或CCL5表達的下調減弱了Ad-Sirt1-MSCs對肝臟炎癥和肝癌發生的促進作用。最后,研究者證明SIRT1通過激活AKT/HIF1α信號軸上調MSC中CCL5的表達。
【3】JAMA Netw Open:警惕!攜帶特定基因突變、且肥胖及過度飲酒會讓個體患肝癌的風險增加近30倍!
doi:10.1001/jamanetworkopen.2022.34221
眾所周知,過度飲酒和肥胖會增加機體患肝硬化和肝癌的風險,但擁有這些因素的個體患病的風險卻并不相同。近日,一篇發表在國際雜志JAMA Network Open上題為“Synergistic Associations of PNPLA3 I148M Variant, Alcohol Intake, and Obesity With Risk of Cirrhosis, Hepatocellular Carcinoma, and Mortality”的研究報告中,來自貝勒醫學院等機構的科學家們通過研究發現,當結合飲酒和肥胖一起考慮時,名為PNPLA3的關鍵遺傳突變風險因素或許在增加機體肝硬化、肝癌和肝臟相關死亡的風險上發揮著一定的協同作用。
文章中,研究人員對來自英國生物樣本庫中40多萬名個體進行了一項前瞻性研究,旨在評估是否PNPLA3突變體的狀態能幫助對肥胖的重度飲酒人群進行疾病風險分類,這些因素中的任何一種都會增加機體患肝病的風險,但研究結果表明,當一個人同時具備上述三種因素時,其患肝病的風險就會大幅增加。
研究者表示,相比未攜帶者而言,攜帶上述三種風險因素的個體患肝硬化的風險是前者的17.5倍,而僅攜帶PNPLA3突變體的個體患肝硬化的風險則是1.75倍,僅肥胖的個體患肝硬化的風險是1.76倍,僅過度飲酒的個體患肝硬化的風險是2.35倍;攜帶這三種風險因素的個體患肝癌的風險是未攜帶者的30.1倍,發生肝臟疾病相關死亡的風險則是21.8倍。
圖片來源:https://jamanetwork.com/journals/jamanetworkopen/fullarticle/2796933
研究者Hyunseok Kim博士說道,PNPLA3突變體對于改善肝臟疾病進展的風險分層至關重要,比如,攜帶PNPLA3突變體的個體會更加積極地接受關于飲酒習慣和BMI的相關資訊,其或許也可能是采取更多預防性措施的候選個體,比如更頻繁地進行篩查以及進行高級別的成像分析。本文研究提供了一個獨特的機會來研究PNPLA3、肥胖和過度飲酒在肝臟疾病風險中的預后作用;研究者Amos表示,我們并不經常會看到這種戲劇性的發現,因此我們對這些結果的臨床意義感到非常興奮。
【4】Science子刊:增加細胞中線粒體和脂質的周轉或能降低機體患肝癌的風險
doi:10.1126/sciadv.abo2510
飲酒和丙肝病毒感染是引發肝細胞癌的已知風險因素,肝細胞癌是一種最常見的肝癌形式;除了這些因素外,肥胖相關的非酒精性脂肪肝如今也逐漸成為西方社會中人群患肝細胞癌的主要促進因素,然而目前研究人員并不清楚肥胖所誘導的肝癌發生背后的分子機制和原因。
近日,一篇發表在國際雜志Science Advances上題為“Lipid droplet turnover at the lysosome inhibits growth of hepatocellular carcinoma in a BNIP3-dependent manner”的研究報告中,來自芝加哥大學等機構的科學家們通過對小鼠模型進行研究后發現,剔除BNIP3蛋白或會降低線粒體和脂滴的周轉率,從而導致脂肪肝發生,最終誘發機體患上肝癌,在人類肝癌中,研究者發現,缺失BNIP3的表達或許與脂質水平增加及患者預后較差直接相關。
研究者Kay Macleod博士說道:“我們的實驗室非常感興趣研究在正常生理狀況下線粒體的功能及其周轉,同時對于癌癥狀況下的相關情況我們也進行了研究。這項研究中,我們發現名為BNIP3的蛋白質或許能作為一種線粒體“貨物受體”。正常情況下,小鼠機體中這種蛋白質在肝臟中的表達會明顯上調從而對禁食產生反應,禁食在保護機體肝臟免于脂肪堆積方面扮演著關鍵作用,然而,剔除該蛋白或許會引發脂肪肝;因此研究人員就想通過進一步研究來理解在正常肝臟和肝癌中BNIP3蛋白的缺失誘發脂質積累的分子機制。”
為了理解BNIP3是如何參與脂質積累的預防以及脂肪肝等狀況,研究人員使用化學致癌劑在兩組小鼠中誘發了肝癌,其中一組是BNIP3完整的小鼠,另一組是BNIP3被剔除的小鼠;研究人員觀察到,在BNIP3剔除的小鼠中,腫瘤發生地較早且生長迅速,此外,這些腫瘤中充滿了脂肪,而在BNIP3完整的小鼠中,腫瘤較小且其中并不含有脂質;當隨著時間延續對這些腫瘤進行追蹤研究后,研究者發現,BNIP3完整的小鼠會發生與BNIP3剔除小鼠相似的脂質堆積現象,更有意思的是,BNIP3的功能已經被沉默了,這或許就表明,隨著疾病的進展,機體或許會出現對BNIP3缺失的選擇。
【5】JNCI:新型藥物組合策略或有望增強肝癌患者機體的抗腫瘤免疫反應
doi:10.1093/jnci/djac051
免疫檢查點阻斷能聯合抗血管生成療法或能誘導血管正常化和機體的抗腫瘤免疫力,對于治療肝細胞癌有一定的療效;但最初的免疫療法是否以及如何影響隨后抗血管生成療法的效率,目前研究人員并不清楚。近日,一篇發表在國際雜志Journal of the National Cancer Institute上題為“Increased CD8+ T-Cell Infiltration and Efficacy for Multikinase Inhibitors after PD-1 Blockade in Hepatocellular Carcinoma”的研究報告中,來自哈佛醫學院等機構的科學家們通過研究開發了一種治療肝細胞癌的新型療法策略,其或能在使用多激酶抑制劑藥物之前,首先利用免疫檢查點抑制劑來處理腫瘤,從而有望幫助治療患這種致命性疾病的患者;研究者指出,這種新型順序方法(sequencing approach)或能增強雙重藥物療法的治療效率,并有可能降低長期使用藥物的程度,從而減少患者毒性藥物的暴露。
研究者Dan G. Duda說道,單獨或聯合使用多激酶抑制劑,隨后再使用免疫檢查點阻斷劑,這種策略歷來能夠檢測治療肝細胞癌患者的療法,然而目前沒有人知道逆轉這些療法的治療順序可能會產生什么樣的影響,于是研究者Duda決定在那些反向非標準順序療法下接受治療的患者進行回顧性的分析來找出答案,當了解到在25名肝細胞癌患者隊列中產生了良好的研究結果后,研究者將其研究擴展到了肝細胞癌小鼠的臨床前模型中,結果發現,首先使用免疫檢查點阻斷療法或能放大宿主機體的免疫反應,這或許會增強藥物索拉非尼(sorafenib)的有效性并產生優越的治療結果,索拉非尼是一種具有抗VEGFR(血管內皮生長因子受體)活性的標準多激酶抑制劑藥物。

圖片來源:https://academic.oup.com/jnci/advance-article-abstract/doi/10.1093/jnci/djac051/6547055?redirectedFrom=fulltext
肝細胞癌是人類所面臨的第二大致命性的癌癥類型,其每年在全球會造成大約70多萬人死亡,同時也是肝癌最常見的形式;早在15年前,藥物索拉非尼就已經成為了治療肝癌的系統性療法,作為一種抗VEGFR抑制劑,其能通過靶向作用滋養腫瘤病促進其進展的血管來控制腫瘤的癌變;就其本身而言,免疫檢查點抑制劑就好像程序性細胞死亡1(PD1)抗體,其能恢復宿主機體免疫系統激活并殺滅癌細胞的能力,在去年一項重大研究發現中,研究者指出,免疫檢查點阻斷或能幫助重編程腫瘤血管中的微環境,當與多激酶抑制劑聯合使用時或許就能導致肝細胞癌中更多的T細胞浸潤和激活,正是這一研究發現或許就能改變免疫檢查點抑制劑和多激酶抑制劑的使用順序,從而就能幫助研究人員在臨床前模型中觀察到會發生什么改變。
【6】Sci Adv:我國科學家繪制原發性肝癌高分辨率空間分子圖譜
doi:10.1126/sciadv.abg3750
異質性是癌癥預防和治療的主要挑戰。近日,我國海軍軍醫大學的研究團隊在Science Advances發表了題為“Comprehensive analysis of spatial architecture in primary liver cancer”的文章。
文章中,研究人員對7例原發性肝癌患者的21個組織樣本進行空間轉錄組學測序,得到84823個位點信息。通過將空間腫瘤微環境特征從非腫瘤區、邊界區到腫瘤區進行漸進式比較,發現腫瘤包膜可能影響腫瘤內空間簇連續性、轉錄組多樣性和免疫細胞浸潤,并且發現腫瘤內部不同細胞亞群具有不同優勢基因表達、細胞功能、預后以及克隆來源,且腫瘤細胞內部亞群并不獨立,在彼此接觸的范圍(100 μm寬交界區)會發生廣泛的配體-受體相互作用,同時發現腫瘤干細胞的富集與原發性肝癌的腫瘤侵襲和遷移呈正相關。通過開發一個新的用于鑒定三級淋巴結構的基因集,他們發現其高評分與原發性肝癌的較好預后顯著相關。
該研究系統分析了腫瘤微環境中不同細胞類型或亞群的空間分布特征,繪制了原發性肝癌的高分辨率空間分子圖譜。
【7】Hepatology:科學家開發出一種有望轉化肝癌免疫療法的新型策略
doi:10.1002/hep.32266
近年來,腫瘤免疫療法已經成為了一種非常有前途且備受關注的腫瘤學方法,其基于利用稱之為免疫檢查點抑制劑(ICIs)的人源化抗體來阻斷抑制T淋巴細胞活性的細胞通路,T淋巴細胞是一類能幫助保護機體抵御感染及癌癥的重要的免疫細胞。最著名的抗體是針對CTLA-4、PD-L1和PD-1的抗體,然而,盡管使用免疫療法治療某些惡性腫瘤已經取得了令人鼓舞的成果,但大多數癌癥患者對使用ICIs的療法仍然反應不佳或根本沒有反應,最明顯的就是肝癌患者。
因此研究人員一直在嘗試尋求新方法來改善免疫療法的治療效率,尤其是通過結合一種以上的療法;目前有多種組合性療法正在進行臨床試驗,但并沒有臨床前數據或明確的理由來證明聯合療法的可信度。近日,一篇發表在國際雜志Hepatology上題為“Enhancing the Therapeutic Efficacy of PD-L1 Antibody for Metastasized Liver Cancer by Overcoming Hepatic Immunotolerance”的研究報告中,來自加利福尼亞大學等機構的科學家們通過研究發現,通過串聯使用一種被稱之為polyIC的合成dsRNA分子來增強肝臟的先天性免疫力,就能使肝癌對一種名為抗PD-L1的免疫檢查點抑制劑產生高度反應。

圖片來源:https://pubmed.ncbi.nlm.nih.gov/34860431/
研究者Feng說道,在開發肝癌免疫療法時我們有兩個問題必須牢記,一般而言,腫瘤微環境的特點是進行免疫抑制,否則腫瘤就不會生長;另一個復雜的層面則是,肝臟是一個獨特的免疫耐受性器官,其會不斷暴露于食物中所獲取的外來物質中,因此,成功的免疫治療必須依賴于克服肝臟的免疫耐受并破壞腫瘤微環境中的免疫逃逸機制。為了解決這些問題,研究人員開發了兩種小鼠腫瘤模型,其中一種是皮膚下生長腫瘤的模型,另一種則是肝臟內生長腫瘤的模型;這兩種類型的腫瘤都來自于相同的結直腸癌細胞系,其能幫助研究人員特異性地調查不同腫瘤微環境所扮演的角色。
【8】Cell Metabol:科學家或能通過靶向作用肝細胞癌的超強代謝能力來開發新型抗癌療法
doi:10.1016/j.cmet.2022.06.010
肝細胞癌是一種典型的致命性惡性腫瘤,其能表現出一定的遺傳異質性和有限的治療反應。近日,一篇發表在國際雜志Cell Metabolism上題為“GCN2 inhibition sensitizes arginine-deprived hepatocellular carcinoma cells to senolytic treatment”的研究報告中,來自賓夕法尼亞大學等機構的科學家們通過研究發現,肝癌的快速生長會導致其能量產生和細胞構建過程中的易感性,而這種易感性或能被一種新型組合性療法來有效利用。
這項研究中,研究人員發現,作為最主要的肝癌類型,肝細胞癌能以一種特殊方式來改變其代謝,從而使其更容易受到名為精氨酸的關鍵分子供應中斷的影響,這種精氨酸易感性存在于所有的肝細胞癌患者中,這與引起癌癥發生的特殊遺傳突變無關。研究人員在臨床前實驗中發現,讓肝細胞癌腫瘤缺乏精氨酸并阻斷由此所產生的促生存反應或能讓肝細胞癌處于一種不生長的衰老狀態,其或許能被一種靶向作用衰老細胞的新型藥物所殺死。從本質上來講,研究人員識別出了大多數肝癌的代謝特性,其或能為他們利用已經獲批或正在研發的有效療法治療這些癌癥提供一定的可能性。
肝細胞癌是成年人中最常見的肝癌類型,據美國癌癥研究所數據顯示,肝細胞癌在所有原發性肝癌(這種肝癌起源于肝臟而并不是從其它器官擴散過來的)中占到了大約80%的比例,每年都有大約2.9萬美國人被確診肝細胞癌,而全球大約有100萬人被診斷為這類癌癥,其被認為是由肝炎病毒、酗酒和肥胖所導致的慢性肝炎所引發的。肝細胞癌很少能被治愈,因為其往往是在疾病發展到無法利用手術進行切除時才被診斷出來,此外,能治愈良性疾病的肝臟移植通常對于晚期肝細胞癌患者而言是不可用的,針對肝細胞癌的藥物療法非常有限,而且其幾乎從未被治愈過,因此,研究人員迫切需要研究開發出新型治療性措施。
【9】Nat Sci Rev:科學家揭示人類肝細胞癌的動態表型異質性和多種RNA亞型的進化機制
doi:10.1093/nsr/nwab192
腫瘤內異質性(ITH)是癌癥療法的一個關鍵挑戰,但此前研究都重點集中在基因組改變上,而并未深入分析表型(轉錄組和免疫)的異質性。近日,一篇發表在國際雜志National Science Review上題為“Dynamic phenotypic heterogeneity and the evolution of multiple RNA subtypes in Hepatocellular Carcinoma:the PLANET study”的研究報告中,來自中國科學院等機構的科學家們通過研究描述了肝細胞癌(HCC)中腫瘤異質性的動態基因組藍圖。
肝細胞癌是全球第七大最常見的癌癥類型,但由于其所引發的較高的死亡率而成為全球第四大癌癥相關的死亡原因;令人震驚的是,亞洲人群承擔了不成比例的80%的疾病負擔。盡管科學家們進行了大量努力,但目前并沒有有效的預測性生物標志物來用于肝細胞癌的系統性治療,且針對肝細胞癌的治療效果仍然不佳。
圖片來源:https://academic.oup.com/nsr/advance-article/doi/10.1093/nsr/nwab192/6414014
為此,PLANet研究計劃的啟動就是為了招募前瞻性的肝細胞癌患者隊列,同時研究人員與亞太肝細胞癌試驗組合作,在多個國家開展了該研究計劃;具體而言,PLANet研究旨在理解名為腫瘤內異質性的腫瘤內部的分子多樣性,以及臨床醫生如何利用這種理解來指導對患者的分層和治療,早在2017年,研究人員就發現,肝細胞癌在不同患者中具有廣泛的遺傳性腫瘤內異質性。
當前的研究是基于來自PLANet研究中的4個亞洲國家中67名患者組成的隊列,也是研究人員對肝細胞癌跨多組學數據層面(基因組、轉錄組和免疫學學)的首個腫瘤內異質性研究。研究者發現,相同腫瘤的不同區域或會在遺傳(DNA突變)和轉錄組(RNA表達)方面出現變化,尤其是,他們發現,這種突變的水平在不同的患者機體中是不同的,且超過30%的患者會表現出高轉錄組的腫瘤內異質性,即一個單一的腫瘤或能包含多個轉錄組亞型。
【10】Cancer Res:新發現!抑癌基因p53若持續被激活或會促進人類肝癌發生!
doi:10.1158/0008-5472.CAN-21-4390
p53是癌癥生物學中一種最重要的蛋白質,通常被稱之為“基因組的守護者”,其會被激活用來對諸如DNA損傷等多種細胞壓力產生反應,p53激活會誘導不同的過程,比如受控的細胞死亡,如果一個細胞變得異常,其就能預防其發生癌變以及癌癥進展,正因為如此,p53的突變在癌癥發生過程中極為常見,包括肝細胞癌等。近日,一篇發表在國際雜志Cancer Research上題為“Constitutive activation of the tumor suppressor p53 in hepatocytes paradoxically promotes non-cell autonomous liver carcinogenesis”的研究報告中,來自日本大阪大學等機構的科學家們通過研究觀察到,遭受慢性肝臟疾病(CLD,chronic liver disease)的患者的肝臟細胞中p53的持續激活實際上會促進肝癌的發生。
慢性肝病的發生是由不同的因素所驅動,包括病毒、酒精使用和脂肪堆積等,所有這些因素都會誘導p53的激活,此前研究結果表明,p53在慢性肝病患者的肝臟細胞中會處于持續激活狀態,然而,目前研究人員尚不清楚其在慢性肝病病理生理學機制中扮演著什么樣的角色。研究者Yuki Makino說道,臨床研究數據清楚地表明,p53會在慢性肝病患者的肝臟細胞中處于激活狀態,因為p53是人體如何預防腫瘤形成的一個重要組成部分,其在慢性肝病中扮演的關鍵角色讓其變得非常耐人尋味。
為了解決這一問題,研究人員開發了一種肝臟細胞中p53積累的小鼠模型,這類小鼠模型是通過剔除Mdm2蛋白所產生的,Mdm2是一種負責調節p53表達的特殊蛋白,其能對其進行靶向降解,這些小鼠模型常常會出現肝臟炎癥,且肝細胞凋亡水平較高以及會出現衰老相關的分泌表型(SASP),這是一種細胞會在微環境中產生信號的現象,其會引發臨近細胞發生癌變,實際上,機體中p53積累的小鼠肝臟腫瘤的發生幾率會增加。研究者Tetsuo Takehara說道,我們還觀察到肝臟祖細胞(HPCs)群體會擴張,其具有干細胞樣的特征,當HPCs被分離出來后,對其進行培養,隨后注射在實驗室小鼠的皮下組織,這些動物就會發生腫瘤,這或許就表明,HPCs在p53積累的動物機體肝臟腫瘤形成過程中扮演著關鍵角色。

- 上一篇

European?Radiology:Gd-BOPTA增強肝膽造影在預測肝癌患者肝切除術后肝功能衰竭中的價值
肝切除術后肝衰竭(PHLF)是肝切除術的致命并發癥,也是圍手術期發病率和死亡率的主要原因,還可導致醫療費用增加、住院時間延長和長期生存率下降。盡管手術技術和器械有很多改進,但 PHLF 的發生率仍然在1.2%到32%之間。對于肝細胞癌(HCC)患者來說,大多數患有慢性肝病和肝功能受損,因此進一步增加了PHLF的風險。肝功能儲備良好的患者是手術切除的良好候選者
- 下一篇

European?Radiology:肝癌的局部進展是否都與熱消融有關?
肝細胞癌(HCC)因其高復發率而備受關注,其治療效果及預后均較差。作為眾多HCC治療方法中的一種,熱消融已被一些指南作物重要的根治性治療手段推薦。由于其微創性、可重復性和成本效益,熱消融已被臨床實踐所接受。然而,許多研究表明,熱消融后的無復發生存率低于手術切除,且消融術后局部腫瘤進展(LTP)的發生率(15-20%)高于手術治療(5-10%)。 LTP是一種
