Nature Cancer:三聯免疫療法有可能治療胰腺癌
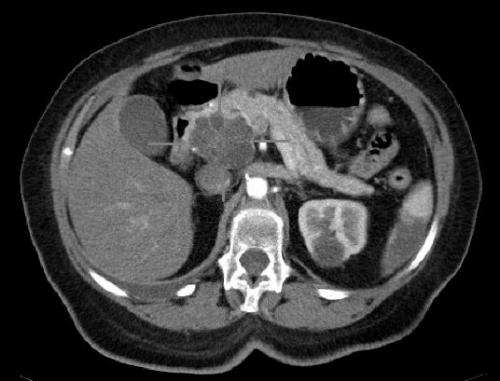
德克薩斯大學MD安德森癌癥中心的研究人員發現了一種新的免疫治療組合,靶向T細胞和骨髓抑制細胞中的檢查點,成功地重新編程了腫瘤免疫微環境(TIME),并顯著改善了胰腺癌臨床前模型中的抗腫瘤反應。
在今天發表在《Nature Cancer》雜志上的這項研究中,研究人員對小鼠和人類胰腺癌進行了全面的免疫分析,系統地確定了免疫治療耐藥的機制,并研究了潛在的治療靶點。他們發現,中和TIME的幾種不同的免疫抑制機制,極大地提高了實驗室模型的存活率,為這種臭名昭著的致命和無反應的癌癥指明了一種潛在的治療方案。
“在我們的模型中,這種三聯療法導致了前所未有的療效反應,”通訊作者、癌癥生物學教授Ronald DePinho博士說。“普遍的觀點是,胰腺癌不受免疫治療的影響,但這項臨床前研究表明,它可能容易受到正確的聯合治療的影響。此外,這些靶點在人類胰腺癌標本中的存在,提出了一種令人興奮的可能性,即這種治療組合有朝一日可以幫助我們的患者。”
胰腺癌是美國癌癥死亡的主要原因之一,部分原因是80%的病例是在晚期被診斷出來的。胰腺癌也被認為是“非免疫原性的”,這意味著它對常用的抗PD-1和抗CTLA-4免疫檢查點抑制劑無反應。這在一定程度上是由于TIME中的免疫抑制條件,但這種耐藥性背后的機制尚不完全清楚。
研究人員使用高維免疫譜分析和單細胞RNA測序來研究各種免疫療法對TIME的影響。他們發現了特定的免疫檢查點蛋白41BB和LAG,它們在耗盡的T細胞中高度表達。
在測試針對這些檢查點的抗體時,研究人員觀察到,與單獨使用抗體或其他檢查點抑制劑相比,使用41BB激動劑和LAG3拮抗劑聯合治療的模型具有更慢的腫瘤進展,更高水平的抗腫瘤免疫指標和顯著提高的生存率。值得注意的是,這些臨床前研究忠實地反映了抗PD-1和抗CTLA-4治療缺乏療效的人類數據。
研究人員還證實,這兩個治療靶點存在于人類胰腺癌樣本中,分別有81%和93%的患者攜帶41BB和LAG3表達的T細胞。
由于這種雙重治療組合并沒有完全消除已建立的腫瘤,研究人員還檢查了重新編程TIME以進一步使腫瘤對免疫治療敏感的努力。在基線時,TIME含有大量表達CXCR2的髓源性抑制細胞(MDSCs), CXCR2是一種與招募免疫抑制細胞相關的蛋白質。僅抑制CXCR2可減少MDSC遷移并阻止腫瘤生長,但不能治愈。這促使研究人員考慮針對41BB、LAG3和CXCR2的組合。
在90%的臨床前模型中,正是這三種組合導致了腫瘤的完全消退和總生存率的提高。在一個更嚴格的實驗室模型中,該組合在超過20%的病例中實現了腫瘤完全消退。
DePinho說:“這些結果令人鼓舞,特別是考慮到胰腺癌缺乏有效的免疫治療方案。通過靶向多種阻礙免疫反應的協同機制,我們可以給T細胞一個攻擊這些腫瘤的戰斗機會。當然,我們仍然需要看看這種組合如何在臨床中轉化為安全有效的治療方案,我們邀請其他研究人員在這些結果的基礎上進行研究。我們樂觀地認為,胰腺癌,以及其他非免疫源性癌癥,最終可以通過聯合免疫治療變得脆弱。”
作者指出,這些特定的免疫療法目前正在作為單一療法進行臨床試驗,這表明有可能將這種三聯療法迅速轉化為臨床研究。

- 上一篇
一種歷史悠久的疾病居然能使肝臟再生!
麻風病是由麻風分枝桿菌引起的一種慢性傳染病,是世界上最古老和最持久的疾病之一。它會影響皮膚、神經和粘膜,如果不及時治療,可能會導致嚴重的毀容和殘疾。然而,新的令人驚訝的研究表明,導致麻風病的細菌可能也有能力刺激成年動物肝臟的生長和再生,而不會造成損害或疤痕。科學家們發現,與麻風病有關的寄生蟲可以重新編程細胞,使肝臟變大。研究結果表明,有可能利用
- 下一篇
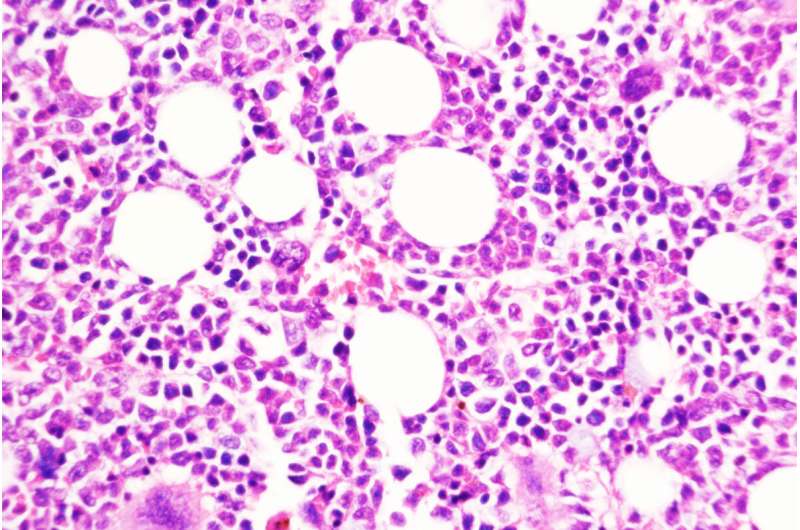
Nature子刊:慢性血癌轉變為侵襲性疾病的關鍵
圣路易斯華盛頓大學醫學院的一項研究提出了一種預防慢性、生長緩慢的血癌發展為侵襲性白血病的策略。圖中顯示的是用一種化合物阻斷DUSP6的小鼠骨髓,DUSP6是由慢性疾病轉變為侵襲性疾病的關鍵分子。一種慢性白血病可以潛伏多年。一些患者可能需要治療來控制這種類型的血液癌癥——骨髓增生性腫瘤(MPN),而另一些患者可能需要經過長時間的觀
