European?Radiology:具有Kupffer期的CEUS在診斷肝癌方面的價值
 全氟丁烷是用于增強超聲成像(CEUS)的第二代造影劑,是一種被Kupffer和網狀內皮細胞吸收的血管后造影劑。除了動態血管增強圖像外,它還能提供Kupffer相(KP)圖像。在KP過程中,肝臟病變中的Kupffer細胞明顯減少或缺失,會出現缺陷。這是與包括六氟化硫在內的純血池造影劑的一個重要區別,后者不通過血管內皮進入細胞周圍間隙,是純粹的血管內造影劑 。由于Kupffer細胞的吸收是在全氟丁烷給藥后約1分鐘開始的,因此微泡不可避免地在血管階段促成了增強。目前還不清楚全氟丁烷增強的US和六氟化硫增強的US在Kupffer細胞攝取方面是否存在不協調的廓清。由于公布的數據有限,美國放射學會發布了2017版CEUS肝臟影像報告和數據系統(LI-RADS),對于使用純血池劑的HCC風險患者,目前版本的CEUS LI-RADS(v2017)并沒有涉及全氟丁烷的使用。目前,CEUS LI-RADS的主要影像特征是否也可能適用于診斷接受全氟丁烷增強的CEUS HCC患者尚不明確。
全氟丁烷是用于增強超聲成像(CEUS)的第二代造影劑,是一種被Kupffer和網狀內皮細胞吸收的血管后造影劑。除了動態血管增強圖像外,它還能提供Kupffer相(KP)圖像。在KP過程中,肝臟病變中的Kupffer細胞明顯減少或缺失,會出現缺陷。這是與包括六氟化硫在內的純血池造影劑的一個重要區別,后者不通過血管內皮進入細胞周圍間隙,是純粹的血管內造影劑 。由于Kupffer細胞的吸收是在全氟丁烷給藥后約1分鐘開始的,因此微泡不可避免地在血管階段促成了增強。目前還不清楚全氟丁烷增強的US和六氟化硫增強的US在Kupffer細胞攝取方面是否存在不協調的廓清。由于公布的數據有限,美國放射學會發布了2017版CEUS肝臟影像報告和數據系統(LI-RADS),對于使用純血池劑的HCC風險患者,目前版本的CEUS LI-RADS(v2017)并沒有涉及全氟丁烷的使用。目前,CEUS LI-RADS的主要影像特征是否也可能適用于診斷接受全氟丁烷增強的CEUS HCC患者尚不明確。
近日,發表在European Radiology雜志的一項研究評估了使用全氟丁烷CEUS對高危患者HCC的診斷性能,并探討與CEUS的傳統診斷標準相比,如何進一步提高全氟丁烷CEUS的診斷及風險分層的準確性。
本研究于013年至2020年期間對在三個機構接受全氟丁烷CEUS檢查的123名高危患者的肝臟結節(≥1厘米)進行了回顧性分析。93%的受試者有病理結果。評估了是否存在動脈期明顯強化(APHE)、廓清時間和程度以及Kupffer期(KP)低強化。KP低強化定義為相對于肝臟KP的低強化病變。HCC的診斷有兩種方式:(1)肝臟影像報告和數據系統(LI-RADS)標準,定義為APHE和晚期(≥60秒)/輕度廓清,以及(2)APHE和Kupffer(AK)標準,定義為APHE和KP低強化病變。本研究探討了導致HCC誤診的灰度特征并反映在調整中。使用McNemar測試比較了診斷性能。
共評估77個HCC、15個非HCC的惡性腫瘤以及31個良性病變。灰階上沒有低回聲暈的邊緣不清晰并不表明為HCC。關于HCC的診斷,AK標準的敏感性(83.1%;95%置信區間[CI]:72.9-90.7%)高于LI-RADS標準(75.3%;95% CI:64.2-84.4%;P = 0.041)。兩組的特異性都是91.3%(95%CI:79.2-97.6%)。
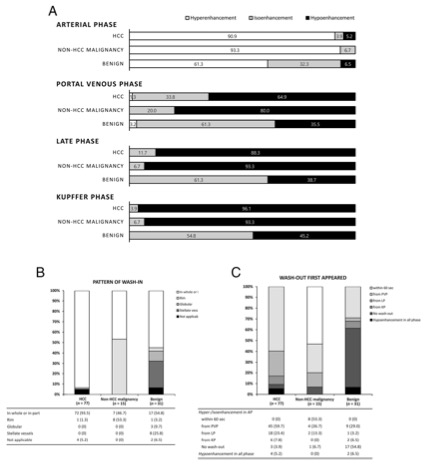
圖 肝臟病變的全氟丁烷CEUS特征。A 肝臟病變在每個期相的結節增強。數值以百分比表示。B 動脈期肝臟病變的廓清模式。C 發生廓清的時間。表中數值以數字(%)表示。HCC,肝細胞癌;AP,動脈期;PVP,門靜脈期;LP,晚期;KP,Kupffer期
本研究表明,并通過灰度結果進行調整,使用APHE和KP第強化的全氟丁烷CEUS HCC診斷標準比APHE和晚期、輕度廓清有更高的診斷性能,且特異性較高。
原文出處:
Jeong Ah Hwang,Woo Kyoung Jeong,Hyo-Jin Kang,et al.Perfluorobutane-enhanced ultrasonography with a Kupffer phase: improved diagnostic sensitivity for hepatocellular carcinoma.DOI:10.1007/s00330-022-08900-6

- 上一篇

European?Radiology:肝癌的局部進展是否都與熱消融有關?
肝細胞癌(HCC)因其高復發率而備受關注,其治療效果及預后均較差。作為眾多HCC治療方法中的一種,熱消融已被一些指南作物重要的根治性治療手段推薦。由于其微創性、可重復性和成本效益,熱消融已被臨床實踐所接受。然而,許多研究表明,熱消融后的無復發生存率低于手術切除,且消融術后局部腫瘤進展(LTP)的發生率(15-20%)高于手術治療(5-10%)。 LTP是一種
- 下一篇

Lancet Oncol:COSMIC-312——肝癌免疫治療之謎
高度異質性的肝癌,對于化療不敏感,靶向治療時代的靶向治療藥物,也只有索拉非尼、侖伐替尼等幾款藥物獲批。免疫治療時代,靶免聯合方案深刻改變了肝癌的治療格局,但隨著LEAP002研究、COSMIC-312研究紛紛失利,重新讓人開始審視不同藥物組合的靶免方案在uHCC上的治療效果為何差異巨大。The Lancet Oncology(IF:59.10)期刊再次提到C
